重度抑郁症(Major depressive disorder, MDD)已成为影响现代人生活最严重的精神疾病之一,对人类健康、经济发展和生活质量带来严重危害。目前,临床上抗抑郁治疗以药物手段为主,但存在起效慢、复发高、治疗响应性差等缺点。深入解析MDD的神经机制,探索新药物干预策略,是治疗抑郁症患者的迫切需求。
研究发现,MDD患者大脑多个区域存在大脑白质纤维束的改变和髓鞘结构异常。多发性硬化症(multiple sclerosis, MS)是一种常见的中枢神经脱髓鞘疾病,数据表明,多数MS患者会出现显著抑郁症状,提示大脑内髓鞘化异常可能参与到MD发病机制。
2022年4月16日,上海交通大学医学院附属精神卫生中心刘芳教授研究团队在医学经典期刊The Journal of Clinical Investigation杂志发表题为:The Eph receptor A4 plays a role in demyelination and depression-related behavior的最近研究成果,揭示了促髓鞘化手段可能作为新型抑郁症干预方案,并证明EphA4可作为相应药物筛选靶点。

结果
1.抑郁症模型小鼠发生髓鞘病变
首先,作者构建了两种不同的抑郁症动物模型:慢性不可预知轻度应激(chronic unpredictable mild stress, CUMS)模拟应激原诱发抑郁样行为;多次脂多糖(lipopolysaccharide, LPS)注射模拟神经炎症引起的抑郁样行为,并借助抑郁相关行为学范式:蔗糖偏好实验(sucrose preference, SPT), 旷场实验(open field, OFT) 和悬尾实验(tail suspension, TST)进行验证。随后,借助免疫组化、LFB髓鞘染色法(Luxol fast blue,LFB)及WB等技术手段发现,抑郁症模型小鼠大脑发生髓鞘病变,存在脱髓鞘现象,表现为:CUMS小鼠腹侧海马髓鞘化(myelination)减少,CUMS小鼠和LPS小鼠腹侧海马中髓鞘碱性蛋白(myelin basic protein, MBP,维持中枢神经系统髓鞘结构和功能的稳定)水平显著降低(图1)。
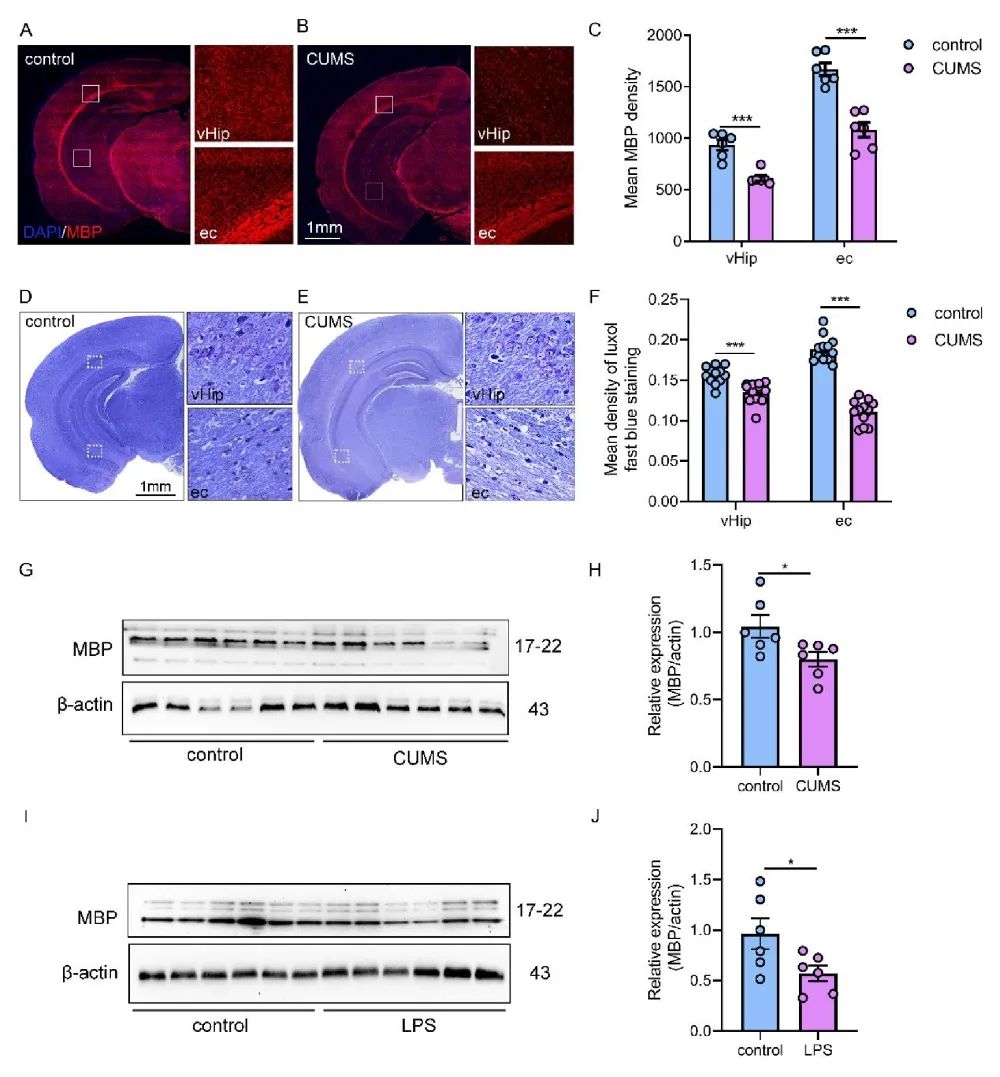
图1 抑郁症模型小鼠发生髓鞘病变
通过对Ranvier节(轴突的绝缘髓鞘有规则间隔的间隙)进行免疫荧光及电镜分析发现,CUMS小鼠腹侧海马的Ranvier节明显长于对照组小鼠,且CUMS小鼠Ranvier节长度分布更广,轴突髓鞘更薄(图2A-G)。此外,WB结果发现,CUMS小鼠和LPS小鼠的突触后致密蛋白-95(postsynaptic density protein-95, PSD95)的表达均显著降低(图2H-K)。这些结果提示了,CUMS和LPS诱导小鼠抑郁样行为,大脑存在脱髓鞘现象,突触蛋白表达降低。
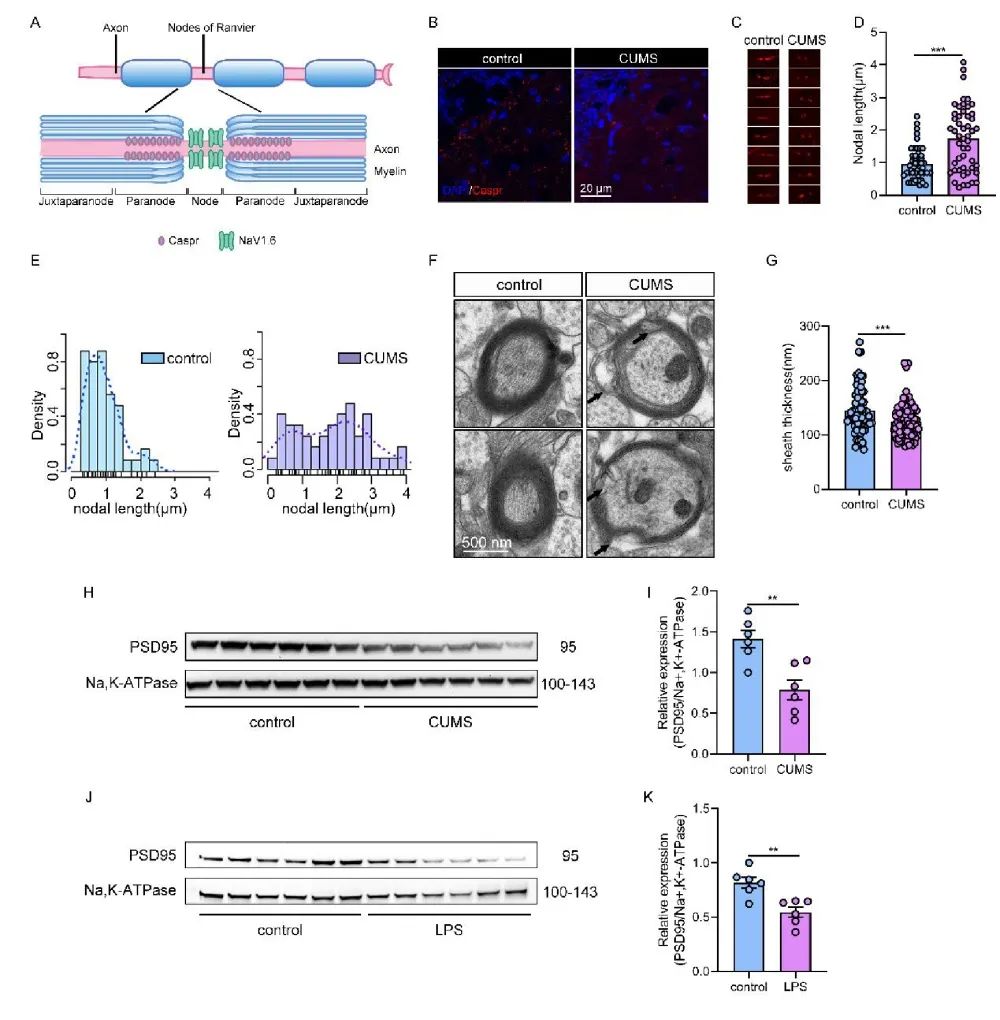
图2 抑郁症模型小鼠大脑存在脱髓鞘和突触蛋白表达降低现象
2.clemastine改善小鼠的抑郁样表型及突触缺陷
基于上述结果,研究团队进一步探究脱髓鞘与小鼠抑郁样行为之间的关系。clemastine(氯马斯汀)为抗组胺药物,在多发性硬化症(multiple sclerosis, MS)患者和MS动物模型中具有重塑髓鞘,促进髓鞘再生的作用。基于此,研究人员连续2周腹腔注射clemastine,行为学结果显示,clemastine改善了CUMS小鼠和LPS小鼠的抑郁样行为(图3A-H)。同时,增加了CUMS小鼠大脑中MBP的表达水平及髓鞘厚度(图3I-O)。

图3 Clemastine改善小鼠抑郁样表型
慢性应激可破坏突触中的局部蛋白合成,导致突触形成、成熟和功能所需蛋白的产生发生改变。研究发现,CUMS小鼠的不对称突触数量减少、突触后致密区厚度变薄,而给予clemastine治疗后,可显著改善这一现象(图4)。提示了clemastine可有效逆转慢性应激引起的突触缺陷。
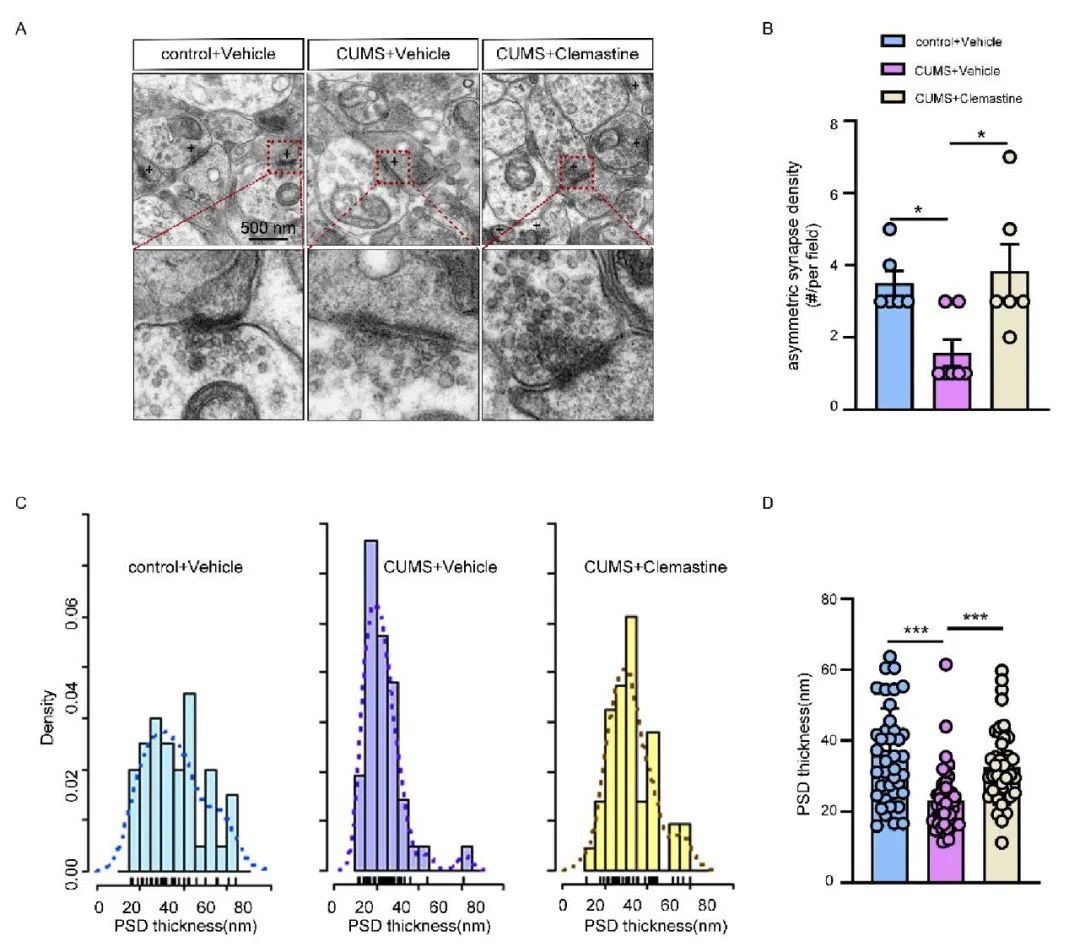
图4 Clemastine改善CUMS小鼠的突触缺陷
3.兴奋性神经元中EphA4的异常表达是导致抑郁症模型小鼠髓鞘病变的重要分子机制
接下来,为发现可能与CUMS小鼠脱髓鞘相关的基因,研究团队基于RNA测序结果及WB分析发现,EphA4的表达在CUMS小鼠和LPS小鼠海马中显著增加(图5A-E)。EphA4是受体型酪氨酸激酶家族中的一个成员,主要在成年海马中表达,参与神经系统发育过程中神经网络的形成、神经再生和突触可塑性。进一步质谱分析发现,CUMS小鼠中EphA4的表达增加可能是其泛素化作用降低的结果(图5F,G)。
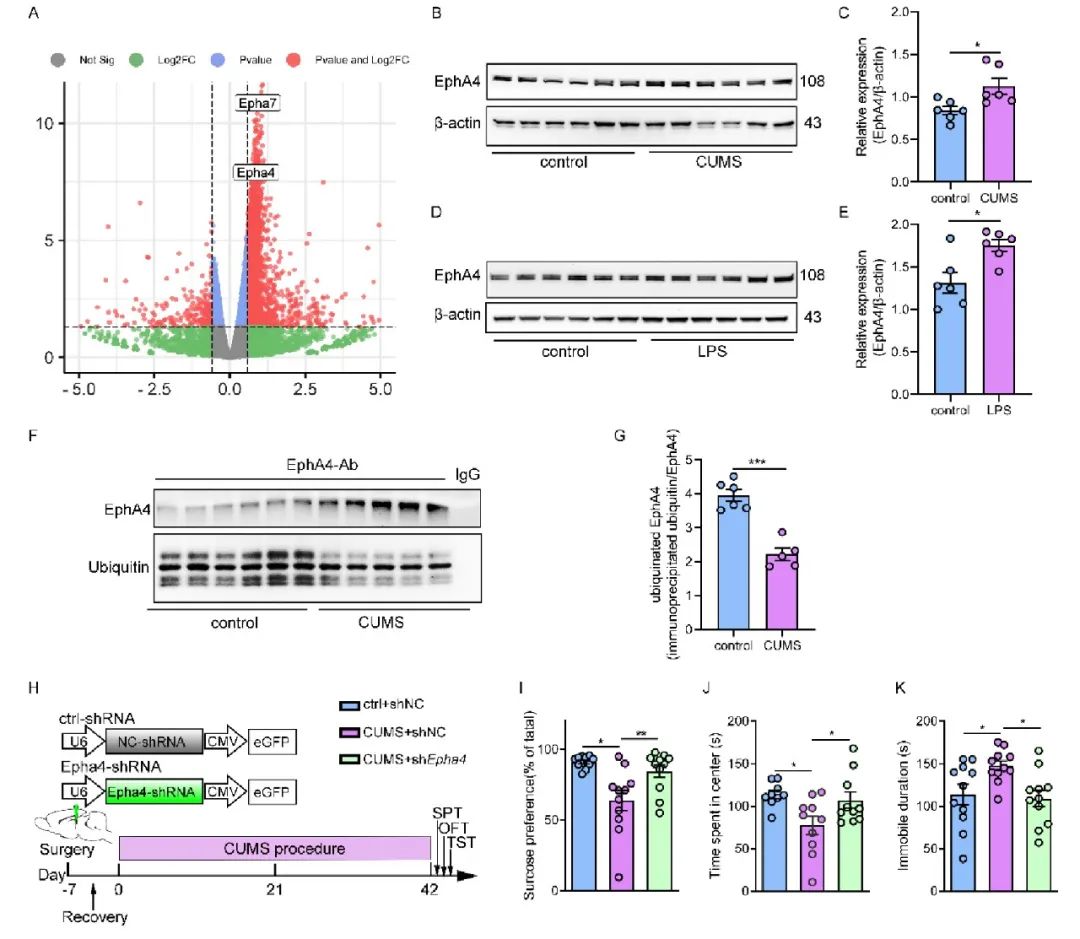
图5 EphA4表达下调可改善CUMS小鼠抑郁样表型
为探究EphA4表达上调与CUMS诱发小鼠抑郁样表型之间的因果关系,研究人员基于基因敲减策略(RNAi技术),在CUMS小鼠海马区注射AAV-EphA4 shRNA,以降低EphA4的表达。蔗糖偏好实验(图5I)、旷场实验(图5J)和悬尾实验(图5K)行为学范式结果显示,EphA4表达下调可有效改善CUMS小鼠的抑郁样行为。同时,EphA4表达下调增加了CUMS小鼠MBP、PSD95和不对称突触数量的表达,以及髓鞘厚度,逆转了CUMS小鼠的突触结构及功能缺陷,促进了髓鞘再生,重塑髓鞘功能(图6)。
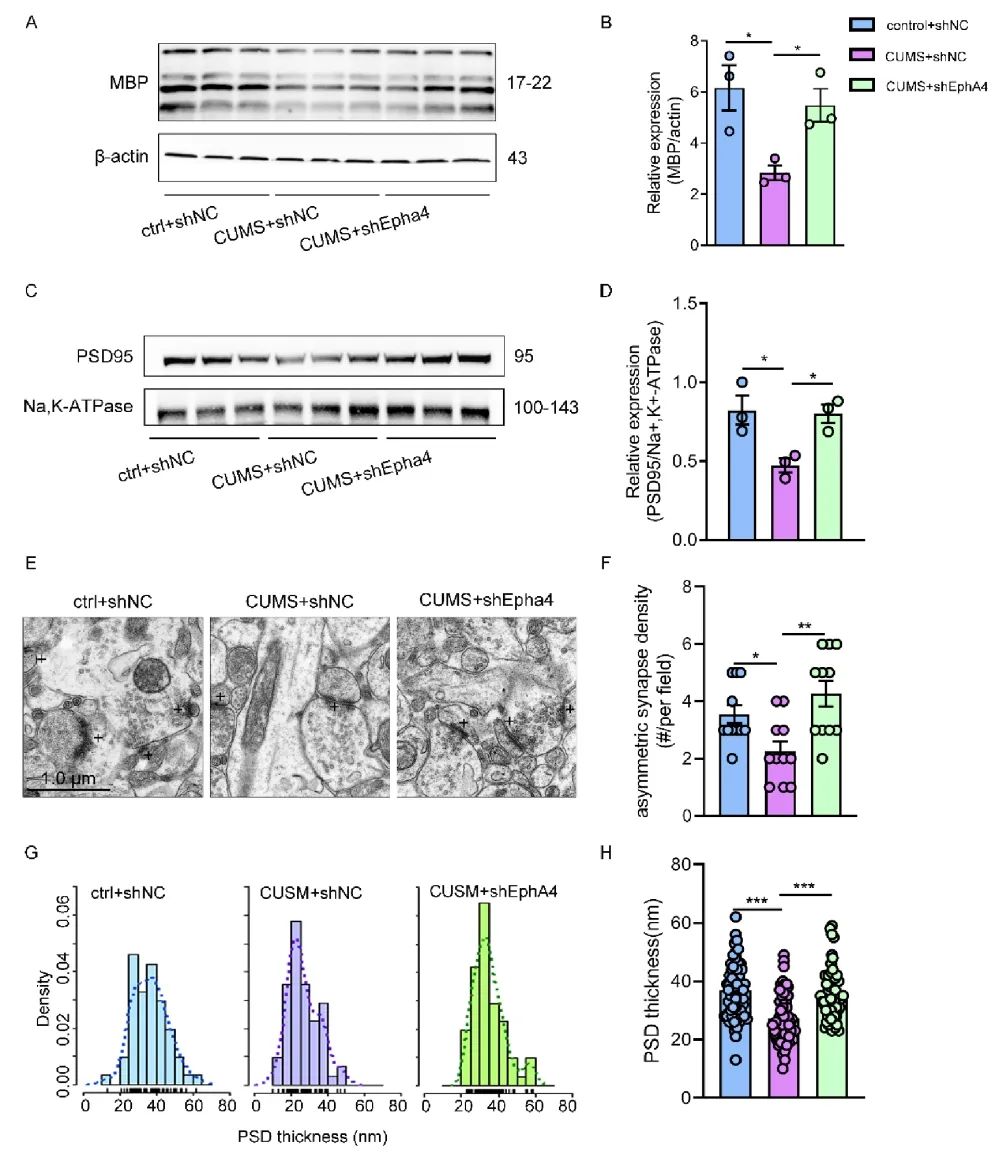
图6 EphA4表达下调改善了CUMS小鼠的突触结构及功能缺陷
EphA4主要表达于兴奋性神经元,且CUMS小鼠兴奋性神经元EphA4的表达显著增加(图7A,B)。作者在CUMS模型小鼠腹侧海马注射pAAV-CaMKIIa-mCherry- EphA4 miR30shRNA病毒载体。结果显示,特异性在兴奋性神经元中敲低EphA4表达可以重塑髓鞘功能和突触稳态,并抑制小鼠抑郁样表型的发生(图7-8)。
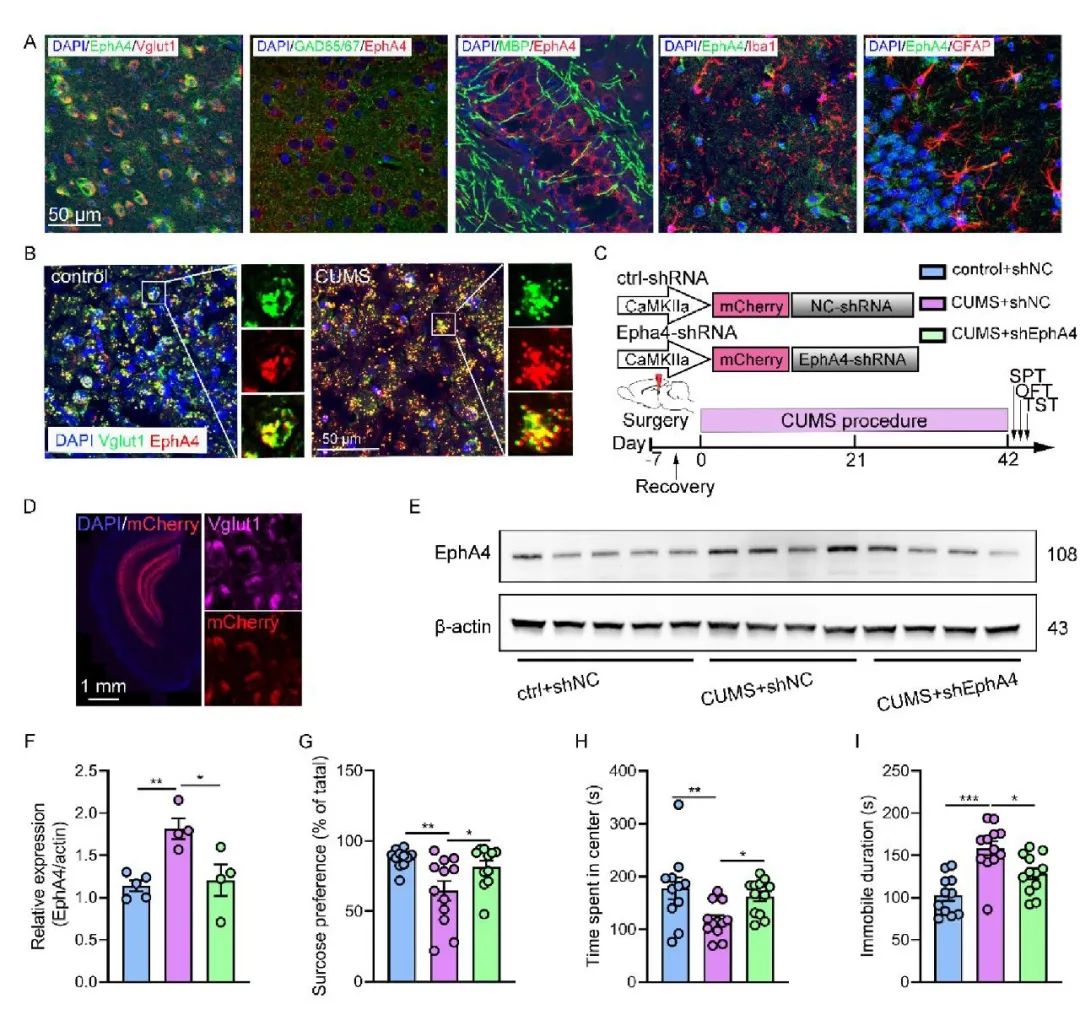
图7 特异性在兴奋性神经元中敲低EphA4表达可以抑制小鼠抑郁样表型的发生
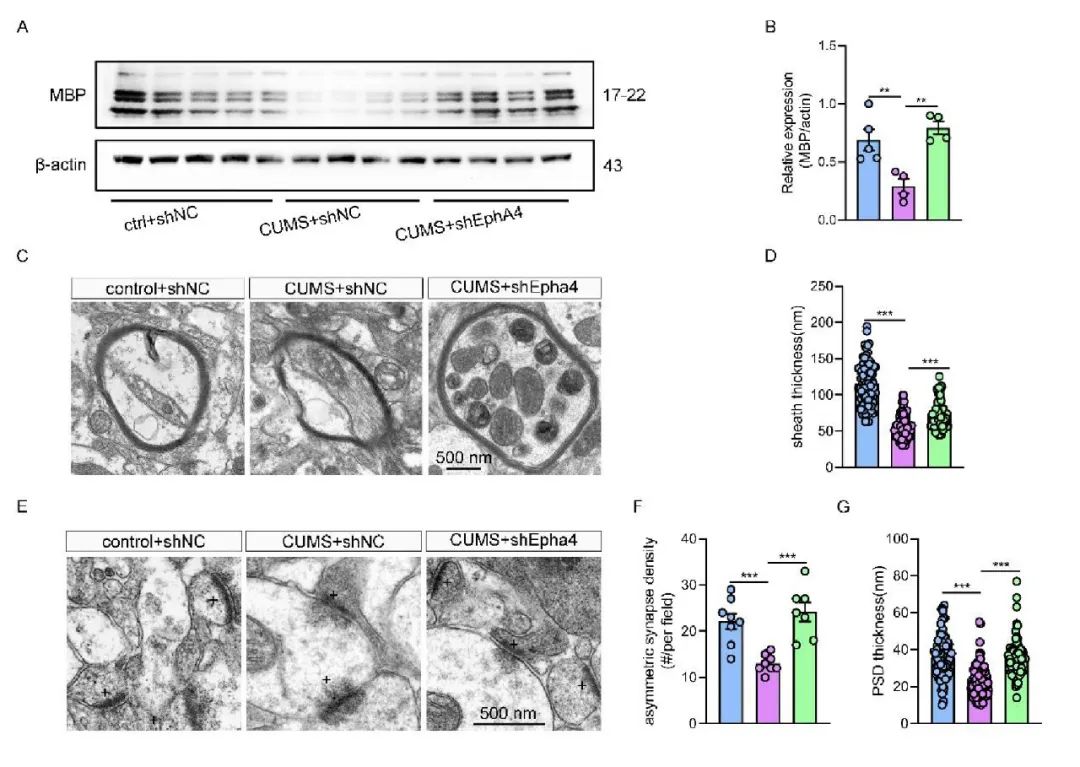
图8 特异性在兴奋性神经元中敲低EphA4表达可以重塑髓鞘功能和突触稳态
4.MDD患者脑组织中存在髓鞘化改变和EphA4的异常表达
为明确该发现的临床意义,研究团队利用人脑库样本同步证实了重度抑郁症(Major depressive disorder, MDD)抑郁患者大脑中MBP和PSD95蛋白显著降低,以及EphA4的异常表达(图9)。这些结果进一步证实了髓鞘化异常在抑郁行为中的重要意义,EphA4可能作为相应药物筛选靶点。
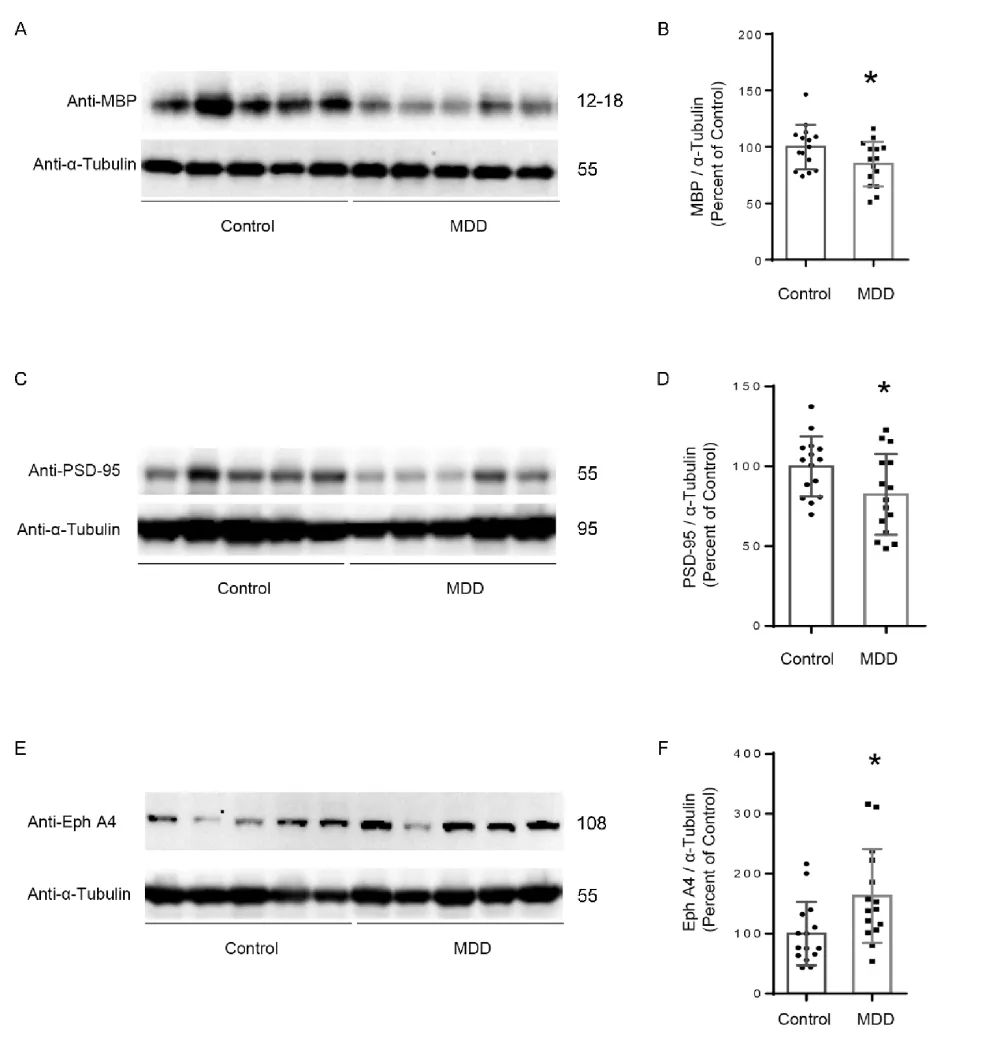
图9 MDD患者脑组织中存在髓鞘化改变和EphA4的异常表达
结论
本文借助CUMS和LPS诱导抑郁症动物模型、多种行为学范式、RNAi技术、转录组、免疫沉淀-质谱分子生物学等多种技术手段,在脑区、环路、单细胞、超微结构、及分子表达上均发现抑郁症模型小鼠大脑存在脱髓鞘现象,进一步研究发现兴奋性神经元中EphA4的异常高表达是该现象的重要分子机制,下调EphA4的表达可促进髓鞘再生、修复突触功能缺陷,抑制小鼠抑郁样表型的发生。同时,临床样本也同步证实了抑郁症患者大脑中髓鞘化改变和EphA4异常高表达。这些证据提示,髓鞘化改变可能是抑郁症的重要病理机制,而EphA4可作为抗抑郁药物研发的新型靶点,为临床上多种促髓鞘化药物在精神医学上的验证提供了理论依据。
和元生物有幸提供实验中使用的AAV载体,用实际行动助力中国脑科学的发展。
原文链接:
https://www.jci.org/articles/view/152187
该论文第一作者为上海交通大学医学院附属精神卫生中心李媛博士,通讯作者为刘芳教授,研究过程中得到了袁逖飞教授的帮助。该项目受到国家自然科学基金的支持。 上海交通大学医学院附属精神卫生中心临床转化研究课题组聚焦神经/精神疾病的细胞分子机制和干预策略研究,特别关注蛋白质-蛋白质相互作用异常对这些疾病发生发展的影响,相关成果已发表于Nature, Cell, Nature Medicine, Neuron, Journal of Clinical Investigation, Biological Psychiatry, Journal of Experimental Medicine和EMBO Journal等高质量杂志中。
课题组长期招聘助理研究员、博士后与科研助理等,有意向者可发送简历至:zmd2012spring@126.com(李老师)
